Spontanicznie przyjmowanym kształtem jest kula. Dlaczego więc płatki śniegu są płaskie, w dodatku powtórzenie struktury następuje co 60 stopni?
Dlaczego płatki śniegu są płaskie?
Pytanie
Odpowiedź
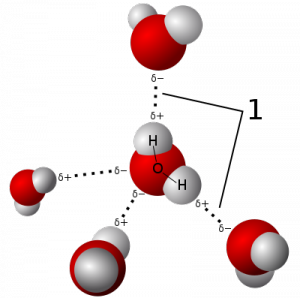
Żaden kształt nie jest przyjmowany spontanicznie, za wszystkie odpowiadają oddziaływania fizyczne. W szczególności, za to jak tworzą się i wzrastają kryształki lodu, odpowiadają siły elektrostatyczne oraz proces dyfuzji pary wodnej w powietrzu. Zacznijmy od budowy cząsteczki wody, pokazanej na tym rysunku (źródło: Wikimedia commons):
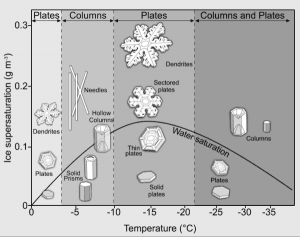
Jak widać jest ona dosyć specyficzna; przez uwspólnienie powłok elektronowych dwóch atomów wodoru i jednego atomu tlenu powstała struktura, gdzie wokół atomu tlenu przeważa ładunek ujemny, a wokół atomów wodoru dodatni. Taka struktura pozwala na wiązanie sąsiednich cząsteczek (co najwyżej czterech) tzw. „wiązaniami wodorowymi”, jak też widać na ilustracji wyżej. Stosunkowo słabe wiązania wodorowe mają krytyczne znaczenie dla wody w stanie ciekłym i stałym. W stanie ciekłym odpowiadają za napięcie powierzchniowe (które skutkuje tym, że w braku ciążenia i oporów objętości wody przybierają kształt kuli). W stanie stałym mają natomiast wpływ na ułożenie cząsteczek wody w sieci krystaliczne, mimo że w takich warunkach cząsteczki wiążą silniejsze wiązania kowalentne. Płatki śniegu powstają wskutek dyfuzji pary wodnej i przyczepianie się kolejnych jej cząsteczek do struktury krystalicznej w ściśle określonych miejscach. Ponieważ kąt rozwarcia cząsteczki wody wynosi ok. 105 stopni (więcej niż 90 stopni), a struktury krystaliczne powstają co najmniej w dwóch warstwach, są one heksagonalne a nie kwadratowe (między cząsteczkami w warstwie może być więcej niż 105 stopni, ale nie mniej). To czy kryształy są płaskie, rosną w „gwiazdki śniegowe”, czy w kształt igieł lub graniastosłupów, zależy od warunków w otoczeniu: temperatury i wilgotności powietrza. Kształt, a precyzyjniej pokrój kryształu (ang. „crystal habit”) jest związany z obecnością słabych wiązań wodorowych, które w różnych warunkach mają różne znaczenie. Wiązania te są wprawdzie takie same, ale przy innej temperaturze – energii kinetycznej cząsteczek, czy wilgotności – gęstości cząsteczek, efekt ich obecności jest nieco inny. W rezultacie mamy bezlik różnych form krystalicznych lodu w chmurach, schematycznie pokazanych tutaj (źródło obrazka: University of Manchester):